基于毛细管驱动微流控技术制造OECT葡萄糖传感器,探索精准且灵敏的血糖监测
2025-12-06 16:53:29 来源:麦姆斯咨询 评论:0 点击:
糖尿病已成为一种影响全球十分之一成年人的代谢性疾病,葡萄糖传感器对于糖尿病管理至关重要。基于酶的生物传感器,特别是那些利用氧化还原酶的传感器,在葡萄糖检测方面具有高度特异性。
据麦姆斯咨询介绍,瑞典林雪平大学的研究团队探索了源自米曲霉的黄素依赖型葡萄糖脱氢酶(AoGDH),并利用了毛细管驱动微流控技术开发无需介质的葡萄糖传感器并将其集成于有机电化学晶体管(OECT)。该研究采用三噻吩单体单元形成与AoGDH连接的导电聚合物,借助黄素腺嘌呤二核苷酸(FAD)辅因子的接近而实现葡萄糖传感。尽管与葡萄糖氧化酶(GOx)相比,AoGDH的稳定性较低,但其不受氧气敏感性影响的特性使其具有优势。通过电化学聚合,研究团队成功将AoGDH整合到OECT栅电极中,尽管是在缓冲溶液中测试,仍实现了生理范围内的葡萄糖检测。相关研究成果已经以“Ad hoc manufactured OECT glucose sensor in capillary-driven microfluidic”为题发表于近期的npj Biosensing期刊。
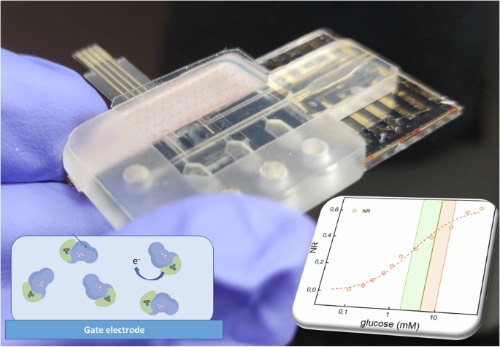
论文摘要附图
虽然FAD-GDH为规避GOx的氧敏感性提供了一种可行的解决方案,但其稳定性较低,这限制了它的广泛适用性。为解决这一问题,研究团队提出在微流控器件内临时按需制造葡萄糖传感器,这样仍能实现便携式测量平台。事实证明,微流控技术不仅是生物传感器系统的一种便捷增强手段,也是辅助检测的一种可能选择。
大多数微流控器件依靠外部流动驱动装置运行,而毛细管驱动的微流控技术则利用毛细作用来调节和牵引液体沿着设计好的微通道流动。这些系统是被动的,不需要电动阀门和泵等外围设备,因此是一种可持续的替代方案,非常适合即时检测应用。此外,采用3D特征能够实现毛细管流动测序这一复杂功能,而3D打印技术使高度定制化的微流控器件成为可能,从而能够针对生物医学应用制造出更复杂的结构。
持续葡萄糖监测技术也受到储存和降解的限制,这也制约了感测产品的制造和运输时间。鉴于该研究通过电聚合进行功能化的方法相对简便,可以在毛细管驱动的微流控器件内实现临时按需制造的葡萄糖传感器。
为了将OECT与微流控器件耦合,研究团队在玻璃基板上制作了金接触OECT,其通道上有PEDOT:PSS,栅电极也位于该基板上。利用一层薄双面胶带将3D打印微流控器件附着到玻璃基板上。电聚合所用的参比电极是一个与微流控器件集成的独立丝网印刷电极。在最初的测试中,研究团队使用了一种单入口的微流控设计,该入口带有确定阻力的结构(毛细管滞留阀,标记为S),以防止微通道排空。因此,入口处的液体在充满微流控通道后会在入口储液器处停止,向该储液器中再加入一滴液体,微流控通道中的流体就会继续流动。通过这种被动的“停-走”方法,可以按需进行功能化、洗涤和葡萄糖测量操作。
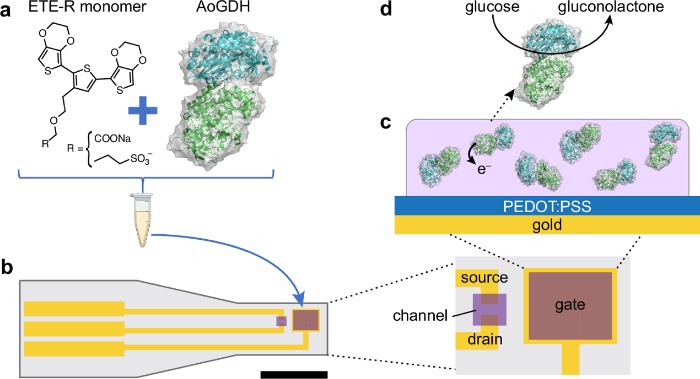
PEDOT:PSS基OECT的功能化
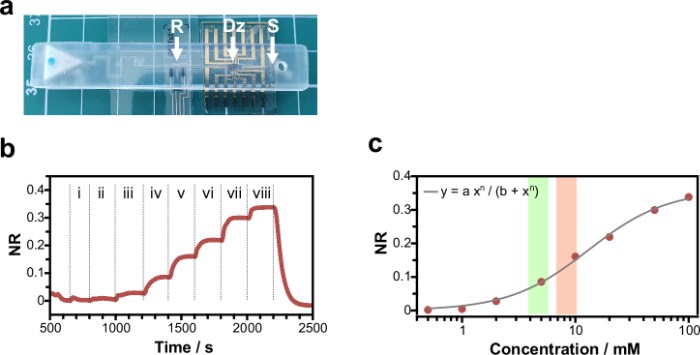
与微流控器件耦合的按需制造OECT传感器
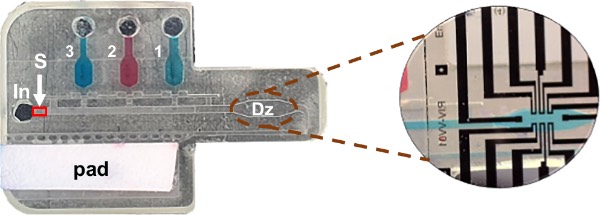
具有预编程序列的微流控器件及其与OECT的集成(放大图)
在添加单体/酶溶液,用OECT填充检测区(Dz)以及放置参比电极(R)贴片之前,先用去离子水对微流控芯片进行泄漏测试。然后,采用计时电流法电聚合对栅电极进行了上述功能化处理。之后,用PBS缓冲液冲洗该系统,获取葡萄糖浓度(0.5–100 mM)下的测量值。结果表面,该系统可以清晰响应感兴趣的葡萄糖生理范围,从5 mM葡萄糖的阶跃变化以及剂量曲线中都能看出。与开放式OECT测量相比,该系统在相同浓度下的响应更低,这可能是由于微流控芯片内部发生了聚合反应。聚合过程中储液器体积较小,或者电极通过细小的液体通道连接(从而引入电阻),都可能影响聚合反应,进而影响剂量曲线。

预编程毛细管驱动微流控芯片的自动释放序列1-3
上图展示了按预编程序列自动输送试剂的微流控器件的时间演变过程。这不仅能实现预编程序列,还能限制储液器向微通道的不必要扩散。其临时按需制造的特点,结合OECT可通过微控制器系统操作,使该技术在即时检测领域具有重要价值,此外,微流控技术还具有仅需微量样本体积的优势。
这种临时按需制作方法能够规避FAD-GDH传感器的稳定性缺点。在该微流控器件中,葡萄糖生理浓度范围可以被清晰检测。此外,该传感器实现了快速的反应时间,这在添加分析物时表现为阶梯状行为。而且,通过在微流控通道上游设置更多具有不同保留能力的储液器(储液器入口),可以对通道内试剂的“自动”释放序列进行预编程。储液器与主微流控通道连接的特殊设计,减少了过早的混合和扩散。
为了得出可靠的人体血糖水平结论,进一步研究以减少检测器件之间的差异至关重要。通过多次连续成膜,有望延长器件的运行时间,实现近乎连续的监测。此外,鉴于该方案可以在电极上靶向沉积,还可以设想构建多电极的传感阵列。综上,该研究强调了基于AoGDH且可临时按需制备的OECT传感器,在生物医学应用中实现精准且灵敏的血糖监测的可行性。
论文链接:https://doi.org/10.1038/s44328-025-00063-w
延伸阅读:
上一篇:突破性微流控平台实现一站式类器官培养与高内涵成像
下一篇:最后一页
