基于重力沉降的微流控器件:从全血中被动分离富血小板血浆(PRP)
2025-09-03 08:35:21 来源:麦姆斯咨询 评论:0 点击:
血小板、红细胞(RBC)、白细胞(WBC)和血浆是全血的主要成分。血小板或血栓细胞是血液中最小的细胞,通过形成血凝块和分泌生长因子来负责止血。这些盘状细胞,通常直径为2~4 μm,厚度为1 μm,在健康成年人血液中的浓度在1.5~4.5 × 10⁵ μL⁻¹之间。
从血液中分离血小板在临床和科研领域有很多实际应用。研究血小板相关的心血管疾病、糖尿病、癌症、免疫、炎症、败血症等疾病的研究方向,通常需要分离血小板进行分析。富血小板血浆(PRP)是一种从血液中提取的自体生物制品,通过促进组织再生和修复来治疗各种疾病。PRP含有血小板浓度高于基础水平的血浆。诊所和医院需要分离和制备PRP用于输血或其它应用,例如伤口愈合、骨骼和组织再生、牙科植入、皮肤再生、头发恢复、生育治疗等。
传统的血小板分离方法包括使用血液成分分离机或PRP与白膜层双离心制备方案。虽然离心法被广泛使用,但由于需要手动步骤和劳动密集型流程,因此操作较复杂。此外,离心可能导致血液污染,分离重复性低,还有不希望的血小板活化。因此,各界正在探索替代方法,以提高效率并减少血小板活化。
根据已有研究报道,微流控器件在血小板回收方面优于传统方法。通常,这些微系统更便携,消耗的样本体积更小,易于自动化,并且由于它们产生的机械应力低于高速离心,因此与传统方法相比显著降低了血小板活化。然而,微流控器件的制造工艺复杂,可能会限制其广泛应用。
此外,也有报道简单、被动式微流控系统,采用重力沉降,能够从全血中分离出高纯度的血浆。重力沉降是一种直接利用血浆和血细胞密度差异的方法。然而,它们采用单沟槽方法,仅设计用于小规模血浆制备(几μL /min量级)。此外,基于沉降的血浆分离器还未在血小板回收和活化方面进行过研究。
利用沉降法,通过多沟槽从全血中提取PRP的器件设计,有望代表一种有前景的解决方案,以克服当前基于沟槽的微系统容量有限的问题,同时保持其高纯度水平。基于沟槽的分离器的主要缺点是气泡形成,因为血液往往无法完全填满沟槽,从而降低效率。为缓解气泡问题,已有研究探索了多种策略,例如疏水屏障、除气和多孔膜等。然而,这些解决方案引入了额外的制造步骤,或要求不适合大规模生产的材料。
据麦姆斯咨询介绍,西班牙巴斯克大学的研究人员开发了一种利用重力沉降原理,从全血中分离PRP的新型多沟槽微流控器件。该器件由一个血液储液池和具有多个矩形、圆形或大沟槽的微通道组成。值得注意的是,这种被动式分离器易于制造,由丙烯酸层和压敏胶(PSA)粘合而成。在沟槽底部使用亲水性压敏粘合剂(PSA)以防止气泡形成。此外,该器件易于操作,仅需使用注射泵即可收集PRP并输送血液。
实验结果表明,该微流控器件可直接从未稀释全血中获得血小板浓度比基线高两倍的PRP,纯度98%,流速12.5 μL /min。最后,测量了血小板活化情况,结果显示使用所开发的器件,血小板完整性优于传统的离心方法。该成果为通过简单且低成本的被动方法获得高质量PRP铺平了道路。相关研究成果已经以“A microfluidic device for passive separation of platelet-rich plasma from whole blood”为题发表于Lab on a Chip期刊。
微流控器件
该PRP分离器由多个通过流体微通道相互连接的陷阱或沟槽组成。研究人员测试了三种不同的沟槽几何形状,以观察对所得PRP的数量、组成和质量的影响。图1a显示了三种研究的器件:第一种有五十个矩形沟槽(1.5 mm x 3 mm x 2 mm),第二种有三十二个圆形沟槽(直径3 mm),第三种有两个大沟槽(40 mm x 3 mm x 2 mm)。连接微通道的尺寸相同(135 mm x 3 mm x 0.3 mm),沟槽数量经过调整以保持相似的死体积,确保三种设计之间有可比的结果。

图1 PRP分离器的结构设计
图1b展示了该器件不同层级的分解视图。每个器件均由流体层和覆盖层组成,通过双面PSA粘合,并在沟槽底部用亲水性PSA薄膜密封。流体层是最复杂的部分,包含沟槽、流体微通道和血液储存室。覆盖层包括移液器进样口、连接注射泵的血液和出料管。血液储存室可容纳1 mL血液,集成在器件中以提高PRP分离的重复性。图1c显示了三个已制造好的器件,每个尺寸为20 mm x 80 mm x 4 mm。分离过程如图1d所示。简而言之,注射泵将血液从芯片上的储存室抽入分离沟槽,血液流经微通道和沟槽,RBC/WBC细胞由于密度较高而沉降。由于流速较低,RBC/WBC细胞被捕获在沟槽底部。最后,分离出的PRP被收集在注射器中。
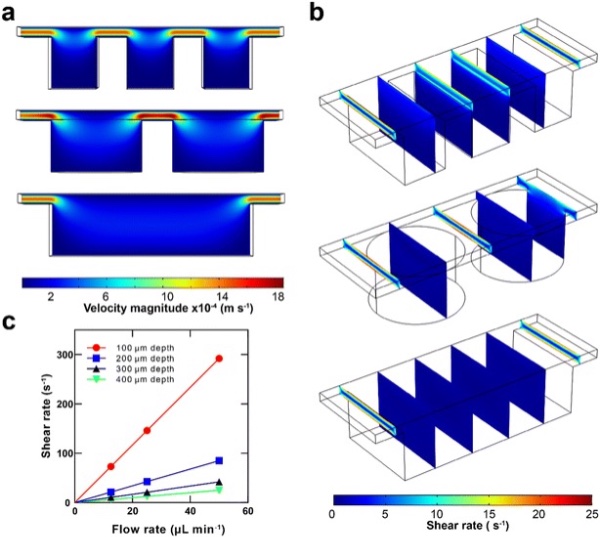
图2 剪切速率和速度仿真
总结而言,研究人员成功开发出一种专为从全血中分离PRP而设计的微流控器件。虽然目前存在其它血液和血浆分离的方法和设备,但本研究专注于开发一种能够高效制备PRP且血小板活化最小的器件,填补了这一重要空白。该微流控器件能够从全血中去除残存的RBC/WBC细胞,且仅使用注射泵操作,无需稀释剂或缓冲液(这些可能会影响PRP的纯度或使其使用变得复杂)。关键的是,该微流控器件的新颖设计通过在分离过程中最小化血小板活化,以保持血小板的品质,而传统方法可能会无意中活化血小板。
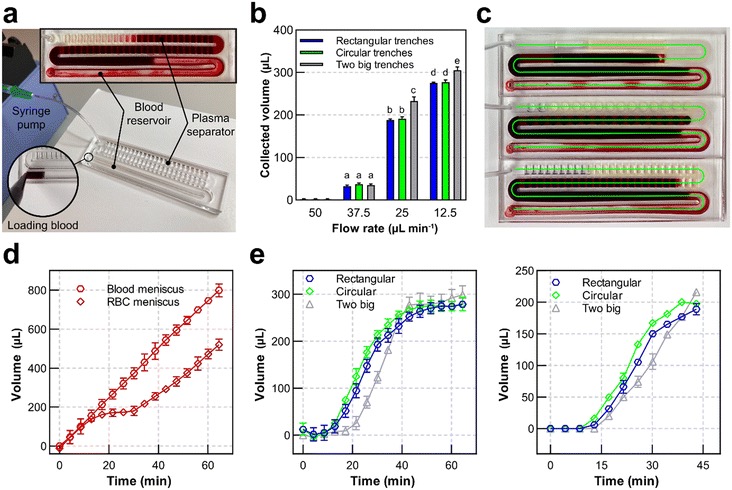
图3 PRP分离结果
研究人员通过流动仿真优化了剪切速率,以改善沉降效果。所开发的方法有效移除了RBC/WBC细胞,纯度分别为98%和96%,处理后仅8.2%的总血小板被活化,而传统离心法的这一数字为31%。该研究成果将新型多沟槽布局、简单性、成本效益和有效的血小板保存相结合,能够批量制造低成本器件,为临床研究和治疗提供所需要的高质量PRP。
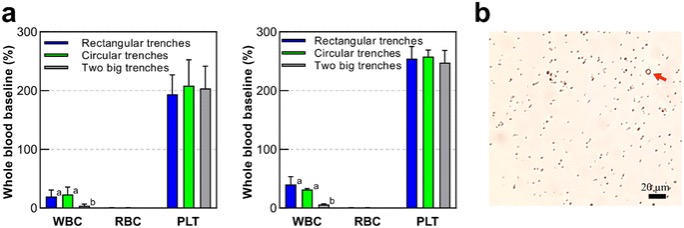
图4 研究中三种器件从全血中分离PRP的血常规分析结果(白细胞、红细胞和血小板)
此外,注射泵可以由其它经济实惠的泵系统替代,例如PDMS真空泵、丙烯酸微泵、低成本蠕动泵或开源注射泵。研究人员认为开发一种专用仪器来操作包含PRP分离器的卡匣是可行的。这些卡匣可以使用文中介绍的方法制造,或通过可扩展的大规模生产技术制造。总之,该微流控器件为高效获取高质量PRP提供了一种直接解决方案,具有制造简单、可扩展且操作适应性强等优势。它作为封闭系统运行,最大限度地降低了污染风险,并消除了对无菌操作设施的需求。
论文信息:DOI: 10.1039/D5LC00362H
延伸阅读:
相关热词搜索:微流控
