突破血脑屏障,利用微流控平台监测胶质母细胞瘤治疗效果
2025-12-23 14:42:09 来源:麦姆斯咨询 评论:0 点击:
胶质母细胞瘤(GBM)是成人中最常见且恶性程度最高的原发性脑肿瘤,目前缺乏有效的治疗方法。数十年来,各界投入了大量研究以改善胶质母细胞瘤患者的预后,但这些努力在很大程度上受到血脑屏障(BBB)的阻碍,限制了药物进入大脑。同时,这些肿瘤对药物的敏感性存在差异,而且由于肿瘤位于脑部,血脑屏障限制了使用循环生物标志物来量化肿瘤负荷或特定治疗的疗效。
识别患者胶质母细胞瘤的动态演变(包括肿瘤进展)通过液体活检可以得到改善,这种方法为肿瘤的系列取样提供了一种非侵入性替代方案。该方法依赖于循环生物标志物的存在,例如释放的肿瘤细胞、无细胞核酸或细胞外囊泡和颗粒(EVP),这些标志物可在各种生物流体(如血浆、唾液、脑脊液)中检测到。然而,迄今为止,在胶质母细胞瘤中使用EVP分析和其他液体活检方法被证明具有挑战性,这可能是由于血脑屏障限制了这些肿瘤特异性生物标志物扩散到外周循环中。
据麦姆斯咨询报道,美国西北大学和密歇根大学的研究团队开发了一种灵敏、快速且经济高效的微流控平台(ᴳˡⁱºExoChip),用于捕获胶质母细胞瘤患者循环中的肿瘤特异性EVP。通过使用GBM细胞系和患者血浆样本,研究团队证明该微流控芯片对肿瘤细胞来源的EVP具有较高的捕获率,且这些捕获物可轻松释放,用于下游表征,如EVP的大小与浓度分析以及蛋白质检测。研究团队利用该芯片对接受紫杉醇(PTX)治疗并伴随血脑屏障开放的胶质母细胞瘤患者EVP动态演变特征进行了表征。相关研究成果已经以“Dynamic release of extracellular particles after opening of the blood-brain barrier predicts glioblastoma susceptibility to paclitaxel”为题发表于近期的Nature Communications期刊。
用于捕获胶质母细胞瘤来源EVP的ᴳˡⁱºExoChip开发与验证
研究团队设计并验证了一种基于磷脂酰丝氨酸(PS)表达来捕获胶质母细胞瘤特异性EVP的微流控平台,并将其命名为ᴳˡⁱºExoChip。研究团队推断,专门从GBM肿瘤细胞中捕获这些EVP,可提高对临床相关信号的检测,并且在多个数据时间点进行动态收集,能够识别与治疗和患者预后相关的时间模式。当液体(如血浆)流过聚二甲基硅氧烷(PDMS)和载玻片之间的封闭通道时,会捕获EVP(主要是外泌体大小范围内的EVP),而去除了囊泡的液体则从每个装置的远端流出。通过在每个通道底部沉积抗体(这些抗体对目标EVP上表达的特定蛋白质或磷脂具有亲和力),可以分离出癌症特异性EVP。
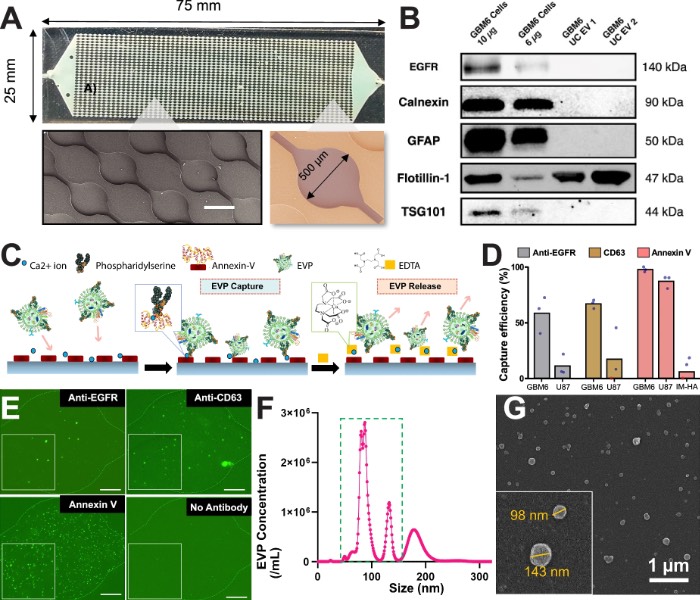
图1 利用GBM细胞系EVP设计和验证ᴳˡⁱºExoChip。该微流控芯片由PDMS顶部和载玻片底部制成。其中,每个通道包含相互连接的500 μm直径的孔,以增强EVP的捕获。每个芯片总共有30 x 60个微孔。
通过ᴳˡⁱºExoChip从血浆中分离胶质母细胞瘤患者来源EVP
接下来,研究团队使用胶质母细胞瘤患者的血浆样本测试了ᴳˡⁱºExoChip对EVP的分离效果。研究团队采用两种不同的血浆体积(100 µL或30 µL,稀释至总体积300 µL)处理了四个样本,以确定使用更多的输入材料是否能获得更多信息。与100 µL血浆相比,研究团队从30 µL血浆中获得的EVP浓度相近或更高。因此,研究团队得出结论,使用ᴳˡⁱºExoChip时,30 µL血浆足以提供可检测范围内的EVP。
图2 使用ᴳˡⁱºExoChip从胶质母细胞瘤患者的血浆中分离和鉴定肿瘤来源EVP
图3 胶质母细胞瘤患者来源EVP的表征
总之,研究团队展示了一种高效的微流控平台,用于分离胶质母细胞瘤患者的疾病特异性EVP,并证明在血脑屏障打开后,EVP可预测对紫杉醇(PTX)的反应。将该平台应用于其它场景,如不同的细胞毒性药物和癌症类型,可能会为EVP生物学和患者治疗反应的生物标志物带来新的洞察。通过标准化的收集方案和用于表征的疾病特异性材料的收集,基于EVP的液体活检有望优化恶性胶质瘤患者的管理和治疗效果。
论文链接:https://doi.org/10.1038/s41467-025-65681-4
延伸阅读:
相关热词搜索:微流控
上一篇:综述:生物医学MEMS器件的前景与趋势
下一篇:最后一页
