基于微流控的双模式柔性生理力学传感器,同时感知静态力和动态力
2025-11-12 22:46:17 来源:麦姆斯咨询 评论:0 点击:
化学信号和力学信号等生理信号是人类疾病早期诊断的重要临床指标。近些年,基于新机制、新材料、新结构和新制造工艺开发的可穿戴医疗设备,无疑为人体生理信号的实时监测提供了有效的解决方案,助力应对医疗健康领域的重要挑战。
在各种生理信号监测平台中,微流控技术因其能够在微尺度上精确操控流体,更好地控制分子浓度及其相互作用而脱颖而出。通过将基本功能单元集成到微芯片上,微流控可以实现整个分析过程的自动化,因而在生物和化学生理信号传感领域吸引了广泛关注。然而,微流控技术在生理力学传感方面的潜力仍未被充分探索,阻碍了多参数生理信号在统一微流控平台上的集成。
生理力学信号的检测主要依赖于压阻式、电容式、压电式和摩擦电原理,每种原理都有其独特优势和固有局限。基于微流控技术的生理力学传感器的开发,有潜力扩展传统微流控技术在生物医学领域的应用,进而在单一微流控平台上统一收集力学和生化信号。这将促进生理状态的协同分析,实现多信息融合传感,具有重大价值。
据麦姆斯咨询介绍,重庆大学研究人员在npj Flexible Electronics期刊上发表了一篇题为“Dual-mode flexible physiological mechano-sensor leveraging microfluidic deformation induced liquid-solid interfacial capacitance and triboelectricity”的研究论文。该研究介绍了一种双模式柔性生理力学传感器,利用了微流控形变诱导的液-固界面电容和摩擦电两种效应。与传统的微流控器件不同,该传感器通过集成的电容和摩擦电机制同时感知静态力和动态力。其中,液滴具有双重作用:一方面作为可变形电极,与底部电极形成平行板电容器用于静态力检测,另一方面,作为与聚二甲基硅氧烷(PDMS)摩擦层接触的摩擦电组件,通过电子亲和力差异产生液-固摩擦电效应。该研究通过利用微流控技术的高精度和可扩展特性,对力学传感器的关键参数进行了全面的理论和实验分析,包括几何形状、柱状物数量和末端压力等。
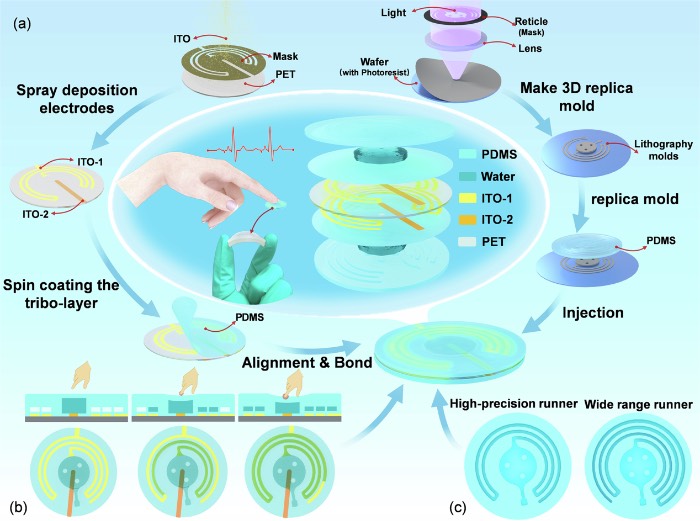
基于微流控的双模式生理力学传感器的结构和基本机制
基于微流控的生理力学传感器的制备与基本结构
这种柔性生理力学传感器的双模式特性,具体在于其同时结合了液-固界面电容和摩擦电机制。这两种机制协同工作,表现为两种不同的功能:高精度静态/动态测量模式,以及自供能动态测量模式。通过精确调节微结构参数,该力学传感器可以实现定制化性能,在测量范围和灵敏度之间取得平衡,在单个器件中兼具高精度和宽测量范围。
这两种模式均包含柔性聚对苯二甲酸乙二醇酯(PET)基板、定制设计的氧化铟锡(ITO)电极、作为介电层和摩擦层的薄PDMS层、带有微柱的传感腔,以及独特设计的PDMS微流控结构层。传感腔通过入口填充水,微流控通道在其末端密封。在外部力不存在时,通道末端的空气压力与腔内水的压力达到平衡。施加压力时,腔室中的水被挤出至微流控通道,与下方的ITO电极形成电容结构。同时,与PDMS层的接触引发摩擦电效应,产生与施加压力成比例的电信号。
这种微流控生理力学传感器的制造采用微加工策略和软光刻技术。其制造过程包括三个主要步骤。首先,选择柔性PET作为基板,通过掩模辅助溅射沉积ITO电极以最小化寄生电容,并旋涂PDMS形成摩擦层来制备底部结构。然后,通过在硅片上使用两步光刻工艺创建PDMS微流控结构层模具,依次定义不同高度的结构,包括传感通道(100 μm)和注射口/传感腔(200 μm)。最后,通过氧等离子体处理将脱模的PDMS结构层与PET基板结合,从而形成微流控网络。
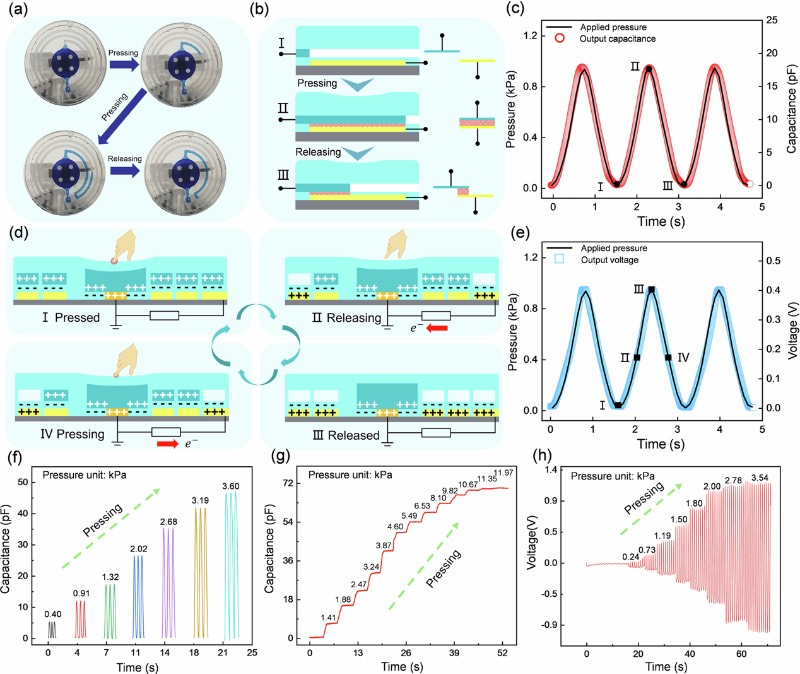
基于微流控的双模式生物力学传感器的原理和传感特性
基于微流控的生理力学传感器在桡动脉脉搏波检测中的应用
由于该力学传感器具有高灵敏度和低检测限,通过腕带将其固定在皮肤表面,在不施加外部压力的情况下成功捕捉到动脉脉搏信号。
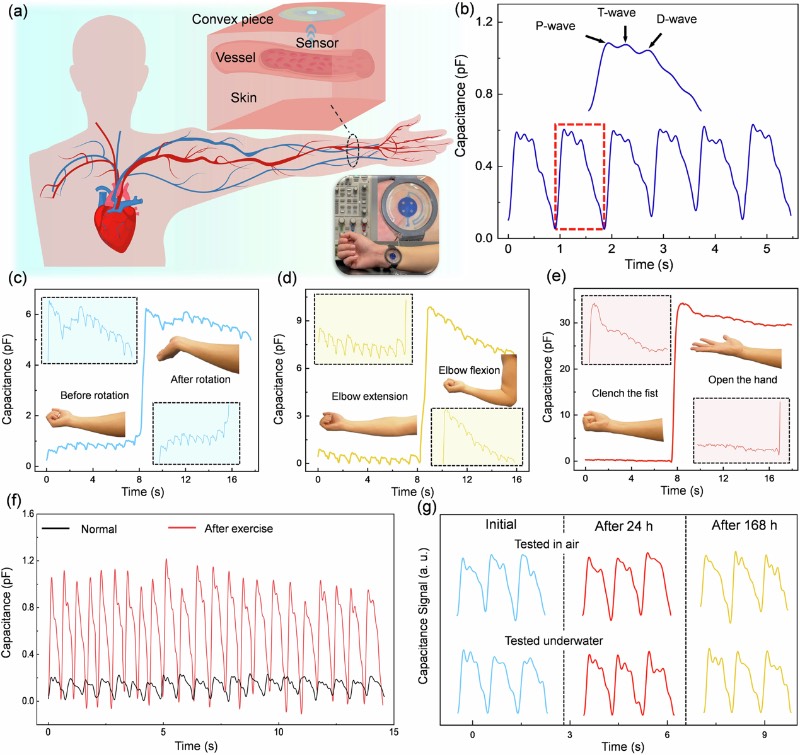
基于微流控的生理力学传感器检测到的桡动脉脉搏波
总结而言,该研究提出了一种利用微流控形变诱导液-固界面电容和摩擦电效应的双模式柔性生理力学传感器。该传感器巧妙地整合了电容和摩擦电检测机制,能够高精度地捕捉静态和动态压力信号,从而超越了传统单一传感技术的局限。通过优化几何参数,传感器在灵敏度(4.078 kPa⁻¹)和检测范围方面实现了协同增强,同时具备21 ms的超快动态响应。此外,摩擦电模式实现了自供电动态检测。
实验验证表明,该力学传感器在空气和水下环境中均表现出优异的线性响应、极小的迟滞和稳健的长期稳定性。因此,它成功实现了长达168小时的高分辨率脉搏监测。这项研究成果为长期非侵入性检测动脉粥样硬化提供了一种极具前景的新方法。
未来的进一步开发将集中扩展压力传感的线性范围,并引入超结构或改性材料以延缓器件传感性能的饱和。同时,通过后端信号处理和机器学习,整合大量数据以减少运动伪影对传感器检测准确性的影响。
展望未来,该平台预计可与生化传感模块集成,促进开发综合的多参数生理监测系统。这种集成有望显著推动可穿戴医疗设备在实时健康监测和精准诊断中的应用。这项研究成果展示了微流控技术在可穿戴设备中集成力学和生化传感的巨大潜力。
论文链接:https://doi.org/10.1038/s41528-025-00487-4
延伸阅读:
上一篇:构建3D有机硅微流控器件新方法:零剂量策略优化体积增材制造
下一篇:最后一页
