微流控纳米等离子体成像平台,用于单个小细胞外囊泡的无纯化和无标记表征
2025-08-10 15:31:00 来源:麦姆斯咨询 评论:0 点击:
小细胞外囊泡(sEV),例如外泌体,通过血液循环在局部及非局部范围发挥细胞间通讯的关键作用。这些囊泡不仅存在于血液中,也存在于几乎所有其它生物体液中。源自内体途径的小细胞外囊泡直径在30至150纳米之间,平均直径约为100纳米。小细胞外囊泡表面蛋白和其内部所含的物质与其细胞来源相关,使其成为研究生物过程的重要对象。精确识别和表征小细胞外囊泡对于探索其在正常生理过程和疾病相关机制中的作用至关重要。传统的小细胞外囊泡表征方法,例如蛋白质印迹、酶联免疫吸附测定和基于微珠的流式细胞术,在评估单个小细胞外囊泡的异质性方面存在显著局限性。此外,这些方法每次检测需要相对较大的生物液体样本量,并不适合小样本输入。更重要的是,这些技术通常需要预先分离和纯化,这些步骤耗时、回收率低且缺乏可重复性,因此将其转化为临床应用仍然存在挑战。
微流控技术通过克服传统流体处理相关的挑战,为分析小细胞外囊泡提供了紧凑、高效及集成化的解决方案。微流控平台能够精确操控小体积样品,并实现自动化样品处理,具有高度可重复性。近年来,微流控系统的创新与光学检测技术的结合,进一步推动了外泌体分析的发展。尽管基于荧光的技术在小细胞外囊泡分析中应用广泛,但这些方法通常需要多种标记和洗涤步骤,涉及荧光染料、量子点或金纳米颗粒,从而增加了检测的复杂性和成本。因此,业界对无标记检测方法的需求日益增长,以降低操作复杂性,保留原始生物结构,避免染料或标记的潜在干扰,并实现不受光漂白影响的实时定量分析。
等离子体传感已成为一种有前景的无标记替代方案,它能够在天然状态下实时分析小细胞外囊泡。据麦姆斯咨询介绍,美国休斯顿大学的一支研究团队不久前开发了一种名为“PlAsmonic NanO-apeRture lAbel-free iMAging(PANORAMA)”的成像技术,专为无标记检测纳米颗粒而设计。该技术利用透明基底上排布的阵列化金纳米盘(AGNIS)上的局域表面等离子体共振(LSPR)来检测小至25 nm的纳米颗粒。AGNIS是在玻璃基底上制造的高密度金纳米盘,具有下凹结构,增强局部电场,并由于辐射耦合产生蓝移的LSPR。AGNIS平台能够利用可见光在复杂生物环境中进行单囊泡检测。
在这项最新的研究中,研究团队将PANORAMA与定制设计的微流控平台相结合,以增强检测自动化、减少样品体积需求,并提高了检测重现性。该装置在微流控通道内采用推拉式流动策略,以优化小细胞外囊泡捕获效率,并提高检测灵敏度。其微流控系统能够精确控制流速、方向、介质体积及组成,从而支持优化的检测条件。微流控-PANORAMA集成平台通过气动方式自动完成整个小细胞外囊泡捕获和检测过程,实现高通量处理,提高了检测准确性。研究人员通过直接在微流控系统内检测和定量血浆来源外泌体,展示了该平台的强大能力。
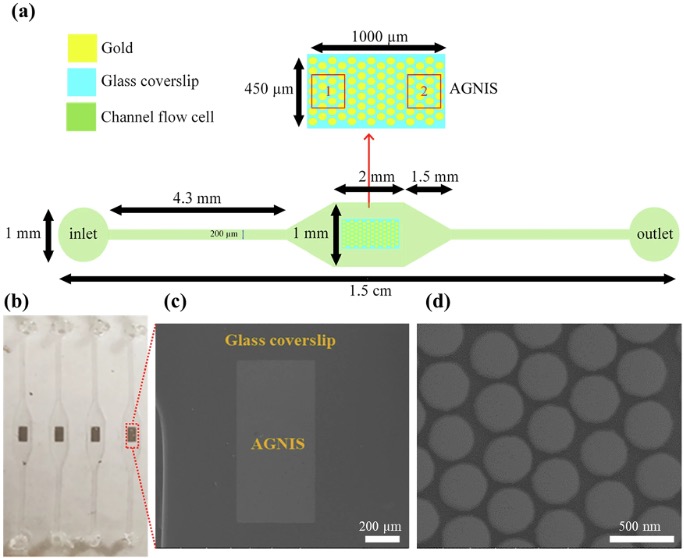
(a)微流控通道设计。(b)AGNIS集成微流控器件的光学图像。(c)微流控通道内单个AGNIS的SEM图像。(d)紧密堆积AGNIS的SEM图像。
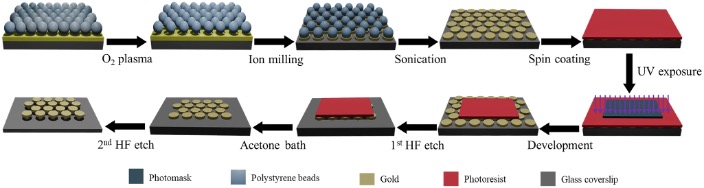
示意图展示了用于与微流控通道集成的矩形AGNIS的制造步骤
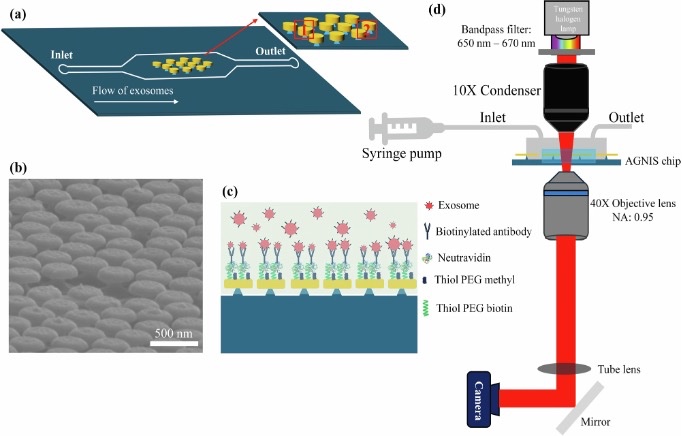
微流控纳米等离子体成像平台概览。(a)微流控器件的概念图。(b)AGNIS表面的SEM图像。(c)用于从人血浆中捕获外泌体的AGNIS表面功能化示意图。(d)微流控器件集成PANORAMA光学装置示意图。
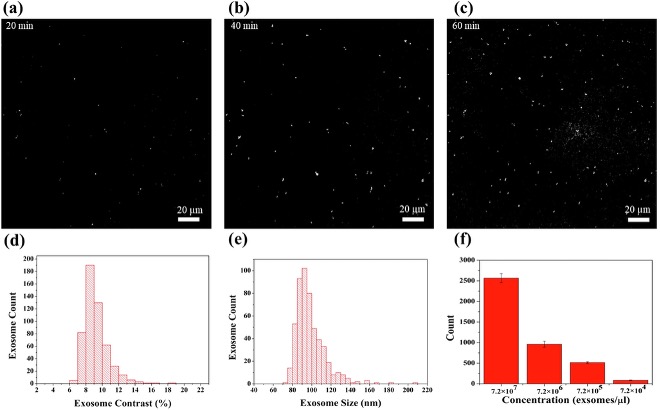
利用微流控-PANORAMA集成平台检测纯化的外泌体
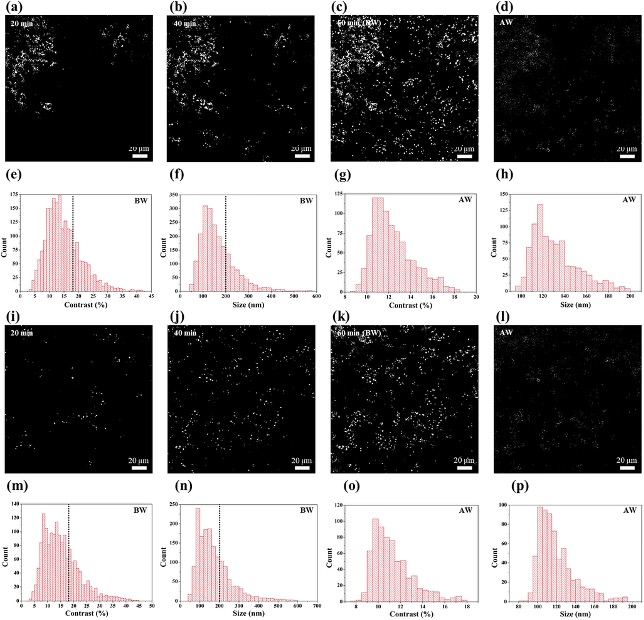
PANORAMA成像用于小细胞外囊泡检测
总结而言,本研究展示了利用集成的自动化微流控系统,通过PANORAMA技术对纯化外泌体及小细胞外囊泡进行无纯化和无标记检测、计数、尺寸表征。在微流控器件中采用推拉流动孵育策略,增强了抗体与血浆样本之间的相互作用,从而实现了外泌体/小细胞外囊泡的高效捕获。仅需20 µL的样本,即可在人类血浆中捕获、检测和计数纯化外泌体/小细胞外囊泡,并具有统计重现性。该平台能够直接从未经处理的血浆中检测小细胞外囊泡,结合其样本需求量小、高灵敏度和无标记操作的特点,表明其在基础外泌体/小细胞外囊泡研究和临床应用中的潜力。
通过多个独立制备和功能化的器件获得的一致结果,验证了该平台的重现性和特异性。然而,该研究的一个关键限制是所有基于血浆的实验都使用了来自同一患者的样本,未评估个体间的生物学差异。尽管这项研究的主要目标是验证平台在受控条件下的可行性和鲁棒性,但未来的工作将涉及更大、更多样化的临床样本集,这对于完全确立其普适性和转化潜力至关重要。
论文链接:https://doi.org/10.1038/s44328-025-00047-w
延伸阅读:
上一篇:面向毛细微流控芯片分析的深度学习分割框架:AI-CMCA
下一篇:最后一页
