深穿透+宽视场+超低功耗,实时3D超声成像开启便携诊断新时代
2026-02-07 21:10:04 来源:麦姆斯咨询 评论:0 点击:
与X射线、计算机断层扫描(CT)和磁共振成像(MRI)相比,超声检查作为一种更安全、成本更低的成像方式被广泛应用。然而,对于可附着/可穿戴形式的贴片式超声设备,尽管已有研究提出了制造适形阵列的方法,探索了新型声学耦合材料,并展示了超声作为X射线乳腺摄影诊断替代方案的潜力,但超声换能器错位问题仍然是一项根本性的挑战。直接的解决方案是广角体积成像,然而现有的3D视频成像架构存在关键的权衡问题,获取此类图像需要过多的O(N²)通道数量、庞大的电子设备以及较高的功耗。
因此,要实现便携式实时3D超声成像以提高其普及性,必须解决三个关键挑战。首先,需要一种稀疏阵列结构,能够在使用最少通道数的同时提供高图像分辨率和宽视场(FOV)。其次,需要一种电子和信号处理方法,以补偿此类阵列的低信噪比(SNR),同时使用低电压并降低功耗。第三,需要一种频率压缩技术,以进一步降低数据采集和处理负担。
据麦姆斯咨询介绍,美国麻省理工学院(MIT)的研究人员提出了一种全新的端到端4D超声架构,其中包括一个带有分立发射(TX)和接收(RX)子阵列的盒形阵列,该阵列与电子模拟前端协同开发而成。该前端采用连续波发射和低频接收电路,在大幅提高信噪比的同时,功耗低于标准超声成像系统。研究人员采用线性调频激励来压缩频率信息,降低模数转换器(ADC)和数据传输的需求,从而实现向图形处理器(GPU)的低延迟实时数据传输,以进行实时图像重建。相关研究成果已经以“Real-Time 3D Ultrasound Imaging with an Ultra-Sparse, Low Power Architecture”为题发表于近期的Advanced Healthcare Materials期刊。
卷积最优分布阵列(CODA)设计
为了满足高稀疏阵列在深度和宽视场成像方面的需求,研究人员开发了一种盒形阵列,其发射和接收子阵列分立且正交。这些发射和接收子阵列的卷积定义了一个有效的声学孔径,即“虚拟阵列”,其大小和分布决定了成像分辨率。该CODA的声学孔径没有重复采样,也没有间隙,意味着它能以最小的伪影获得最清晰的远场图像分辨率。小型元件具有宽角度灵敏度,能够对超出阵列覆盖范围的区域进行成像。因此,该CODA仅需O(4N)个元件,就能实现与O(N²)个元件的全矩阵阵列相同的宽视场成像和远场分辨率。
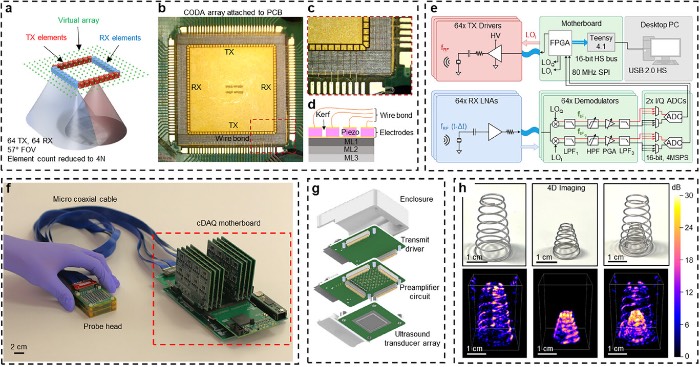
图1 实时3D超声成像系统架构:(a)CODA设计的概念图,包含专用发射和接收元件以及相应的均匀采样“虚拟阵列”。(b)实际的CODA,具有64个发射和64个接收元件,安装在载体PCB上。(c)CODA的放大视图,显示元件几何结构和引线键合。(d)CODA的侧视示意图,显示三个匹配层、实心底部接地电极、经过机械加工的压电陶瓷和顶部电极。(e)cDAQ的框图,显示发射驱动器(红色)和接收低噪声放大器(蓝色),通过微型同轴电缆连接到主板(绿色)。主板包含对接收信号执行下变频、滤波、放大和采样的模块。(f)cDAQ系统照片,包括通过微型同轴电缆连接到主板的探头。(g)探头分解图。(h)通过CODA和cDAQ系统获取的锥形弹簧的照片及相应的体积超声图像。
本研究制作的CODA包含128个阵元,其孔径尺寸与1024阵元的全矩阵阵列相当,总阵元数量减少了8倍,接收阵元数量减少了16倍。为此,研究人员开发了一种定制的微加工工艺,利用超快激光从480 μm厚的单晶铌镁酸铅-钛酸铅(PMN-PT)材料中制造该阵列。阵列表面层压了三层匹配层,形成指数锥形的声阻抗分布,阵列阵元通过引线键合连接到载体印刷电路板(PCB)。
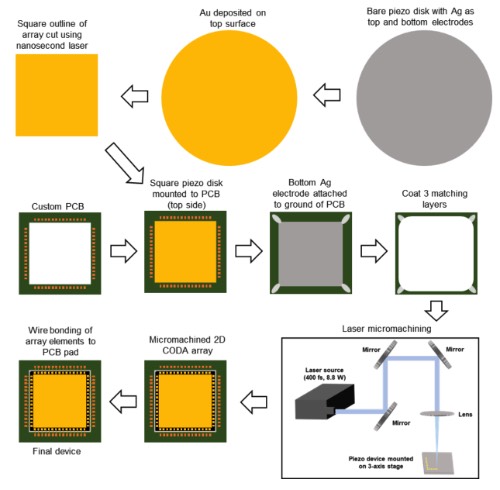
图2 CODA超声阵列制造工艺

图3 1D和2D CODA阵列显微图像
啁啾调制数据采集系统(cDAQ)设计
为了应对信噪比挑战,研究人员开发了一种新的“啁啾调制数据采集”(cDAQ)超声架构。该架构利用压缩感知原理,在低系统电压下提高信噪比,同时将采样率降低两个数量级。从本质上讲,这项技术通过对接收信号频率进行下变频、无源滤波,最后以降低的速率进行采样,在模拟域中执行信号平均操作,完全避免了能耗高的过采样和数字抽取。因此,虽然CODA将耗电的接收通道数量减少了16倍,但cDAQ架构使每个通道的功耗进一步成倍降低了1.85倍,与同等的全矩阵阵列相比,总功耗降低了29.6倍。
软组织的实时3D成像演示
研究人员展示了cDAQ和CODA系统在生物组织成像方面的能力,首先对乳腺肿瘤体模进行体外成像,然后,对人体乳腺组织进行了体内成像。为了进行对比,研究人员使用Verasonic脉冲系统搭配L11-5v线阵探头获取了B模式图像。在体内测试中,招募了一名女性受试者,其右侧乳房约2-3厘米深处有多个充满液体的囊肿。研究人员使用相同的两套系统和探头对囊肿进行成像,探头在乳房上的放置位置相同。实测图像表明,cDAQ和CODA系统能够成功定位囊肿。此外,在cDAQ获取的图像中,与L11-5v获取的图像相比,囊肿看起来更深且形状更接近球形。与L11-5v探头相比,CODA探头的面板表面积更大,因此导致乳腺组织的机械变形更小。这对于长期监测应用而言非常重要,因为放置引起的变形会因操作者而异,并会降低在多个检查时段对比图像的能力。在成像过程中保持囊肿形状完好至关重要,特别是对于乳腺癌检测等应用,以便量化肿瘤大小随时间的变化。
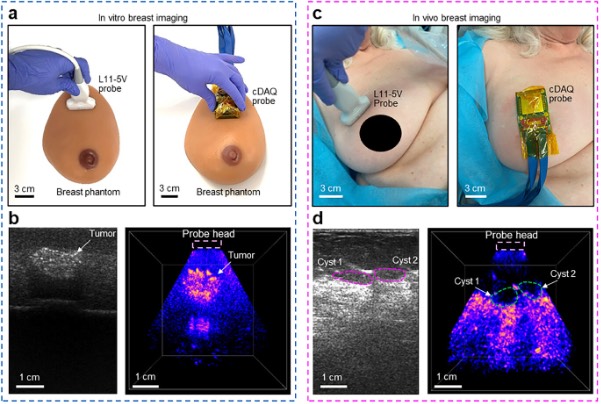
图4 对乳腺体模的体外研究和对乳腺组织的体内研究
结论
该研究提出了一种端到端的4D超声架构,该架构包含一种新型稀疏阵列几何结构和协同设计的数据采集系统。其CODA阵列实现了宽视场(57°)成像,同时将阵元数量从O(N²)减少到O(4N),简化了制造过程,使高分辨率体积成像更具实用性。同时,与市售产品相比,cDAQ将所需电压和采样率降低了一个多数量级,并且将每通道功耗降低了近一半。此外,整个系统(包括阵列、电缆和数据采集电子设备)总重量仅为1.15磅,使其成为一款完全便携的超声成像系统,具有更高的实用性。系统性的体外表征和乳腺囊肿的体内成像表明,该系统非常适合软组织器官成像,且组织变形极小。所提出的架构方法实现了高性能、实时3D超声成像,为下一代医疗设备消除了一个关键且长期存在的障碍。
论文链接:https://doi.org/10.1002/adhm.202505310
延伸阅读:
《压电式微机械超声换能器(PMUT)期刊文献检索与分析-2022版》
上一篇:AlN压电MEMS器件噪声的建模与测量
下一篇:最后一页
