利用微流控“痛觉芯片”识别慢性疼痛类型,让疼痛感知不再主观
2025-04-15 14:44:38 来源:麦姆斯咨询 评论:0 点击:
慢性疼痛是一项全球性的健康问题,人们对它知之甚少,治疗起来也很困难。要改进疼痛的分类和治疗,就必须采取新的策略,客观区分疼痛状况,并尽量减少与疼痛感知相关的主观因素。
例如,就诊时告诉医生到底有多疼一直是个难题。为此,澳大利亚莫纳什大学(Monash University)的研究人员开发出了一种巧妙的解决方案,可以让疼痛诊断不再靠猜测。
据麦姆斯咨询报道,莫纳什大学的研究人员开发了一种被称为“痛觉芯片(pain-on-a-chip)”的新型微流控生物传感器,它可以客观地区分不同类型的慢性疼痛,例如纤维肌痛和糖尿病神经病变等。
这项突破性技术是由莫纳什大学与弗林德斯大学(Flinders University)合作开发的,其工作原理是在微型芯片上分析活体感觉神经。
在该研究中,研究人员探索了一种基于痛觉感受器的微流控生物传感器,被称为“痛觉芯片”,用于区分从表型不同的慢性疼痛临床前模型中提取的血清样本。
研究人员介绍了“痛觉芯片”生物传感器的微流控模型,以及该装置适应类似痛觉感受器50B11细胞分化和功能验证的能力。50B11细胞是一种常用于神经科学研究的永生化感觉神经元细胞系,通常来源于大鼠或小鼠的背根神经节(DRG)。这类细胞经过基因改造(如SV40大T抗原转染)实现永生化,保留了部分感觉神经元的特性,广泛应用于疼痛机制、神经再生、药物筛选等研究领域。
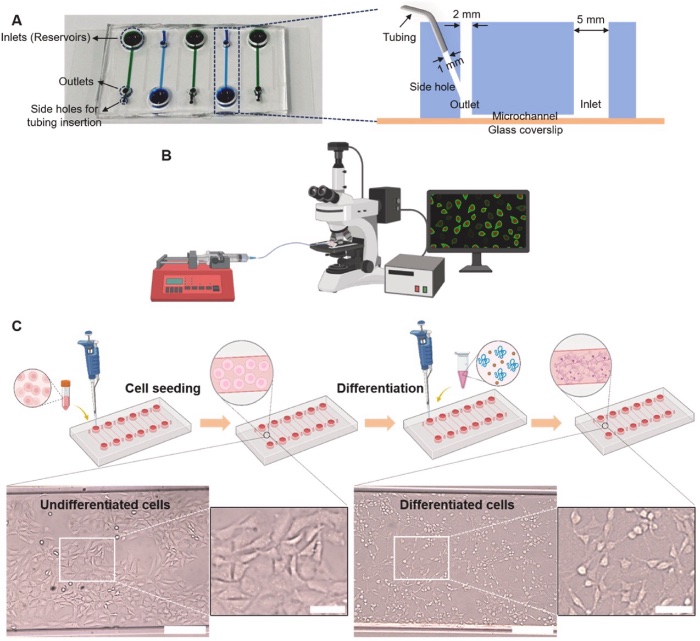
(A)微流控“痛觉芯片”示意图;(B)通过泵灌注刺激剂,促进片上Ca²⁺成像;(C)50B11细胞在微流控芯片系统中的播种和分化过程。
该模型的目标细胞被称为“痛觉感受器”,它们能启动痛觉,与各种慢性疼痛病症有关。通过观察这些细胞对血液样本的反应,研究人员可以在临床前研究中区分纤维肌痛引起的疼痛和糖尿病神经病变引起的疼痛。
该“痛觉芯片”针对小容量血清样本的功能分析进行了优化,拓宽了可检测与痛觉相关的可溶性介质的液体范围。该研究包括单通道芯片模型的初步开发,然后推进到多通道芯片模型,以实现各种细胞亚型(例如未分化与两种分化亚型)的共培养、分化和同步功能验证。
通过活细胞成像评估和量化细胞内钙离子(Ca²⁺)水平的增加来监测痛觉感受器的兴奋。通过分析Ca²⁺信号模式对ATP和辣椒素等激动剂刺激的反应,检验了“痛觉芯片”的功能性。
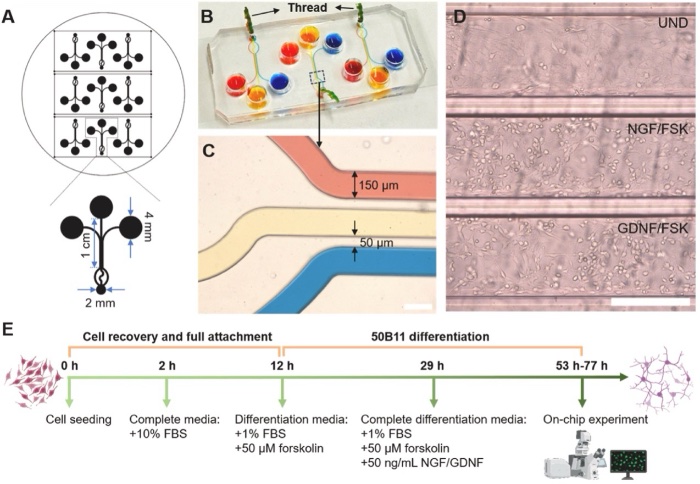
(A)、(B)和(C)用于不同细胞类型共培养和同步成像的三通道复用芯片的设计和尺寸示意图;(B)和(C)采用亲水纤维保持介质单向流动,避免不同细胞介质混合;(D)在EVOS FL Auto 2显微镜下拍摄的实际细胞形态图像,进一步验证了三通道之间的有效区分和分离;(E)UND 50B11 细胞分化为NGF/FSK和GDNF/FSK亚型的时间轴。
最后,研究人员检测了两种不同慢性疼痛大鼠模型的血清样本。即使血清样本的体积很小,这种“痛觉芯片”系统也能在对照组和两种慢性疼痛大鼠模型之间显示出统计学上的显著差异,从而证明了它作为一种客观方法的潜力,可以在类似痛觉感受器的基于细胞的微流控系统中区分表型不同的生物流体。
这种“痛觉芯片”概念有可能为微创和客观分析方法提供一种生物传感器平台,以区分慢性疼痛亚型。
这对于那些难以表达自己疼痛程度或可能被视为主观症状的患者来说,有望改善他们的生活质量。
弗林德斯大学的Dusan Matusica博士解释说:“由纤维肌痛和神经病变等疾病引起的慢性疼痛,可能会让人感到非常孤独,而且极度虚弱。”
这项研究为开发一种基于血液采样的客观判别工具奠定了基础,利用该微流控模型可以确定慢性疼痛状态。目前在临床前和临床应用中都缺少这样一套诊断工具。
同样来自莫纳什大学的副教授Nicholas Veldhuis希望这项技术能继续向临床应用发展。最终提供一种能改善慢性疼痛患者生活的器件。
论文链接:https://doi.org/10.1016/j.bios.2025.117401
延伸阅读:
