利用两步消耗微流控方法,从血液中有效分离稀有细胞
2025-03-30 21:35:58 来源:麦姆斯咨询 评论:0 点击:
间充质基质细胞(MSC)因其在治疗方面的潜力以及作为疾病生物标志物的作用而极具前景。尽管已有证据表明,外周血(PB)中存在循环脂肪源性间充质基质细胞(c-ASC),但要将它们分离出来却极具挑战,这是因为其在外周血中的含量极低、细胞尺寸存在差异,并且它们在外周血中的天然免疫表型尚未完全明确。因此,血液中脂肪源性间充质基质细胞(ASC)的频率与各种生理或病理状况之间的关系尚未得到充分研究探索。
据麦姆斯咨询报道,近日,图卢兹大学(Université de Toulouse)、图卢兹大学 RESTORE 研究中心、图卢兹生物技术研究所(Toulouse Biotechnology Institute,TBI)以及法国国家科学研究中心(Centre National de la Recherche Scientifique,CNRS)的研究人员介绍了一种名为ASC-Finder的无标记分离方法,该方法专门用于分离脂肪源性间充质基质细胞(ASC)——这是一种关键的间充质基质细胞(MSC)。相关研究论文以“Isolation of adipose stromal cells from blood using a two-step microfluidic platform ASC-finder”为题发表在Nature期刊上。
ASC-Finder集成了两个独立的模块:一个是基于尺寸的流体动力学过滤模块,该流体动力学过滤模块能够直接从外周血中筛选出红细胞;另一个是基于免疫标记的阴性富集模块,可用于去除残留的白细胞。该装置能够高效去除99.98%的红细胞,同时在稀有细胞浓度下对掺入的ASC实现高于81%的高回收率。这项研究工作代表了在不进行细胞裂解的前提下,从全外周血中直接富集ASC技术上的重大突破,为深入研究循环于血液中的ASC的特征和功能作用,迈出了至关重要的一步。
间充质基质细胞是多能基质细胞,能够分化为脂肪细胞、成骨细胞和软骨细胞。间充质基质细胞存在于骨髓和其它多种组织中,具有显著的免疫调节特性,能够在组织修复和免疫调节过程中发挥重要的支撑作用。
到目前为止,由于面临着一系列的挑战,标准分离技术一直难以有效地从血液中分离出循环于血液中的c-ASC:(1)c-ASC在血液中很少见,每毫升血液中c-ASC的数量从几个到数百个不等;(2)这些细胞的尺寸分布范围较广,直径在10至20微米之间;(3)它们缺乏特定的独特膜标志物,使其识别变得复杂;(4)包括该研究团队尚未发表的研究成果在内的多项研究均表明,ASC可能与血小板或白细胞形成细胞群并在血液中循环流动。此外,由于在像血液这样复杂的介质中,最先进的流式细胞术检测灵敏度有限,因此利用该技术检测稀有细胞也存在较大的困难。因此,要想在血液中ASC的浓度与特定生理或病理生理状态之间建立起可靠的相关性,极具挑战,这也导致目前已报告的数据存在可靠性欠佳,一致性不足的问题。
微流控技术或许能够满足这一基本需求,并且由于其能够对流体流动进行精确控制,能够有效地操纵稀有细胞,因此成为分离c-ASC的理想技术选择。
在这项工作中,研究人员提出了一种两步消耗微流控方法(ASC-Finder),该方法能够从血液中分离并收集浓度低至68±35 ASC/mL的 c-ASC,为在各种病理或炎症条件下对c-ASC进行定性和定量分析奠定了基础。这项研究成果有助于更深入地理解c-ASC在代谢障碍中的作用,并确定c-ASC是否能够作为代谢障碍或其它病理状况的预测指标。此外,该研究还能够为稀有细胞分析领域提供支持,有助于发现此前未被注意到的稀有循环细胞亚群,从而推动常规诊断装置的研发工作。
ASC-Finder介绍
ASC-Finder回收装置由两个消耗模块组成(如图1)。第一个模块是基于尺寸的分选单元,能够有效地去除直径小于10微米的细胞,这些细胞主要是红细胞、血小板以及较小的白细胞。由于红细胞在血液成分中占比超过99%,因此对红细胞的去除操作会在很大程度上影响c-ASC的高效分离。研究人员选择了流体动力学过滤技术,因为该技术非常适合处理复杂的介质样本,并且无需对样本进行额外的预处理操作。第二个模块是基于标记的“Y-Y”磁泳分离模块,该模块利用功能化的抗白细胞共同抗原抗体(anti-CD45)磁珠,去除样本中残留的白细胞。
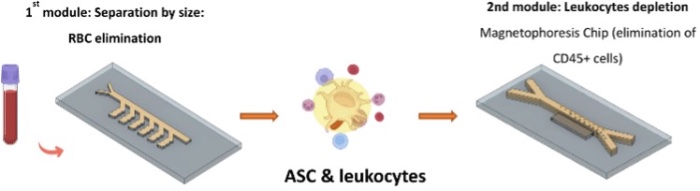
图1 用于从全血样本中分离ASC的ASC-Finder装置,该装置由两个模块组成:(1)基于尺寸的过滤模块;(2)基于标记的分离模块。
流体动力学过滤(HDF)模块
流体动力学过滤的工作原理如图2a所示。简单来说,如果研究人员研究在一个由主通道和单个侧通道组成的通道网络中流动的流体,那么通过侧通道的那部分流体会在主通道中定义一条虚拟的分隔线。这条虚拟分割线到通道壁的距离决定了芯片的截留能力Rc。这种基于尺寸的排阻现象之所以会发生,是因为任何中心位置处于虚拟分割线和主通道侧壁之间的颗粒,都会通过侧通道流出,从而被过滤掉。而直径大于临界尺寸(R>Rc)的颗粒将留在主通道内,并通过主出口流出。
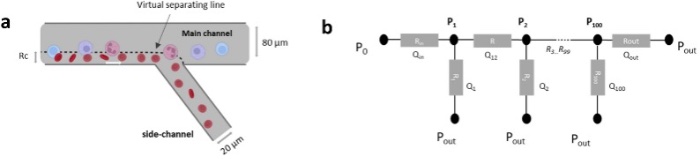
图2 流体动力学过滤(HDF)微型芯片介绍
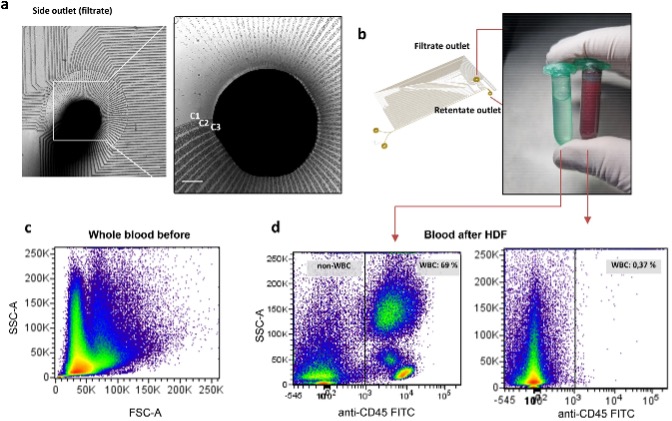
图3 第一个模块:全血过滤实验
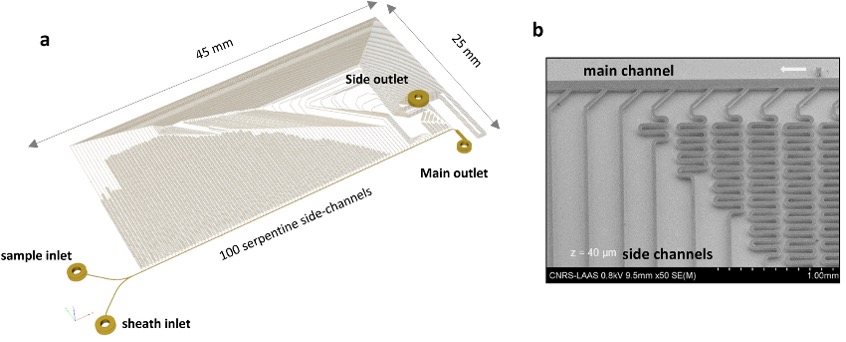
图4 流体动力学过滤(HDF)微型芯片
磁泳模块
第二个模块包含一个磁泳单元,其功能是在磁场的作用下,对磁性颗粒进行选择性分离。磁泳技术与微流控技术的耦合应用,在相关文献中已有大量的详细描述。
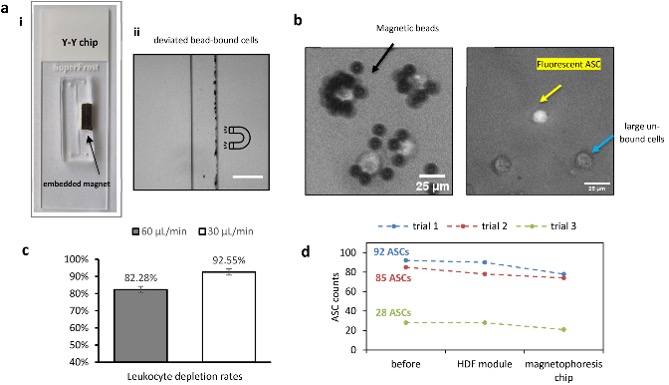
图5 磁泳模块及其实验
尽管该研究的长期目标包括使用糖尿病或其它疾病小鼠模型的实验,但在初始阶段引入这些模型会带来一些混杂变量,这是因为在2型糖尿病(T2DM)中,c-ASC的行为特性尚未得到充分的表征,并且在不同的小鼠模型中,c-ASC的行为表现可能存在较大差异。因此,在将该装置应用于更为复杂的病理条件之前,在标准化的健康环境中对其进行验证,是确保其可靠性的关键步骤。在进一步深入研究2型糖尿病中c-ASC的动态变化(包括在疾病进展过程中追踪其数量水平,以及评估其功能潜力等方面)之前,这种基础的验证工作对于保证研究结果的准确性和一致性至关重要。
最重要的是,该研究结果表明,在经过关键的流体动力学过滤(HDF)步骤之后,ASC仍然保留了其增殖能力以及分化为脂肪细胞的能力,这是其生物学作用的两个基本方面。这一结果表明,ASC-Finder能够维持稀有c-ASC的功能完整性,从而为大规模的细胞表征研究以及潜在的临床应用提供了一个强大的技术平台。上述研究发现凸显了两步消耗微流控方法在富集低浓度ASC方面的有效性,为稀有细胞分析提供了一个极具价值的工具。对c-ASC进行深入研究的能力,有望加深研究人员对这些稀有细胞群体的认识,以及它们与各种疾病之间的关联,为在研究和临床应用领域实现潜在的突破创造条件。
论文链接:https://www.nature.com/articles/s41598-025-94353-y
延伸阅读:
上一篇:“微生物学+微流控”新研究表明:要克服抗生素耐药性,必须让抗生素“流动”起来
下一篇:利用级联粘弹性微流控技术,从未稀释血液中分选多种循环肿瘤细胞
